LEY DE BOYLE - MARIOTTE (fundamento)
Un gas ideal es aquel que
cumple unas condiciones determinadas expresadas en forma de leyes simples, que
veremos a continuación. Muchos gases se comportan como ideales a baja presión.
Históricamente, la primera de
las leyes de los gases ideales se debe al inglés Boyle y al francés Mariotte e
indica que, para una temperatura determinada, el producto de la presión P por el volumen V de un gas permanece constante K:
P V = K
Por tanto, la presión es
inversamente proporcional al volumen o viceversa.
P = K / V
V = K / P
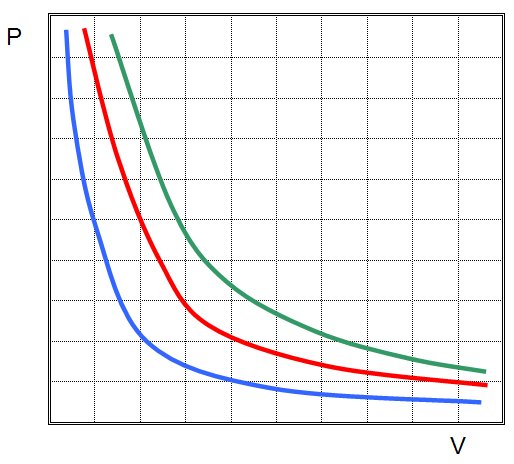
Ambas expresiones
corresponden a la ecuación de una hipérbola. La gráfica muestra líneas de (V,
P) para distintas temperaturas. En cada hipérbola la temperatura permanece
constante y se llama isoterma.